Biosci. Biotechnol. Biochem., 74 (9), 1951-1952, 2010
Poznámka
Izolácia N,N-dimetyl a N-metylserotonín 5-0-¢-glukozidov z nezrelého zanthoxylu •“Reritum Seeds
Emiko YANASE, Masaki OHNO, Hironari HARAKAWA a Shin-ichi NAKATSUKA‘
Fakulta aplikovaných biolagických vied, Gifu Universit y, 7-7 Yanagido, Gifu 501-1193, Japonsko
Prijaté 8. apríla 2010; Prijaté 27. mája 2010; Online publikácia, 7. september 2010 [doi:10.1271/bbb.100261]
Dva deriváty serotonínu, N,N-dimetylserotonín-5-0-Q-glukozid (la) a N-metylserotonín-5-0-Q-glukozid (lb) , boli izolované z nezrelých semien Zanthoxylum piperitum. Ich štruktúra bola určená viacstupňovými konverznými reakciami a spektroskopickými analýzami. Nezrelé semená Z. piperitum obsahovali extrémne vysoké hladiny zlúčenín la a lb, približne 0,29 % a 0,15 % (w/w), v tom poradí.
Kľúčové slová: Zanthoxylum piperitum‘, japonské korenie; N,N-dimetylserotonín 5-0-J9-glukozid; N- metylserotonín 5-0-Q-glukozid
Zanthoxylum piperitum (japonské korenie) je rastlina pôvodom z Japonska a iných častí východnej Ázie. Medzi augustom a septembrom prináša drobné červené plody. Čerstvé mladé listy rastliny, ako aj oplodie sa používajú ako korenie, ktoré v japonskej kuchyni poskytuje sviežu a horkú chuť. Celé nezrelé plody vrátane semien sa používajú ako korenie na tsukudani, ktoré obsahuje tradične konzervované morské plody. Iba oplodie zo zrelých plodov Zanthox ylum bungeanum sa v Číne používa ako žalúdočný liek, analgetikum a korenie. Lesklé čierne semená sa vyhodia alebo ignorujú.
Najznámejšie kultivary Zanthox ylum v Japonsku sú Asakura-sansho, ktorý sa nachádza v Kjóte a Hyogo, a Budo-sansho vo Wakayame. Divoký druh nazývaný Kogen-sansho sa pestuje v oblasti Hida v prefektúre Gifu a má sa za to, že produkuje lepšiu arómu ako ostatné.
Je známe, že hlavnými štipľavými zložkami v tomto ovocí sú shanshool a shanshoolamid 3 a že aromatickými zložkami sú limonén, geraniol atď. 4 O zložkách alebo semenách Zanthox ylum sa však veľa nevie . Preto sme sa pokúsili objasniť zložky prítomné v nezrelých semenách Zanthox ylum , ktoré sa pestovali v oblasti Hida v prefektúre Gifu. Tieto semená boli zozbierané medzi koncom júla a augustom v roku 2007.
Semená (860 g) sa dvakrát extrahovali etylacetátom, aby sa odstránili nepolárne zložky, a potom sa dvakrát extrahovali metanolom, čím sa získal etylacetátový extrakt a metanolový extrakt (13,5 g).
Reverzná fáza HPLC analýzy metanolového extraktu ukázala, že neobsahoval žiadne štipľavé zložky (napr. a-sanshool), ale obsahoval dve vysoko polárne zložky s unikátnou UV absorpciou.
Metanolický extrakt sa prečistí stĺpcovou chromatografiou na silikagéli [MeOH-CHCl-28% vod. NH3—
H20, 50:42:1:7 (obj./obj.) a potom 80:0:4:16 (obj./obj.)], čím sa získa surový la (4,90 g) a surový lb (2,41 g). Analýza pomocou HPLC naznačila, že tieto vzorky boli takmer čisté, ale stále obsahovali určité množstvo minerálnej soli. Vzorky sa preto adsorbovali na kolóne Diaion HP-2055, ktorá sa eluovala metanolom a premyla vodou. Tento proces odstránil minerálnu soľ a potom sa získali zlúčeniny la (2,97 g, čistota > 99 %) a lb (0,53 g, čistota > 99 %) ako bezfarebné tuhé látky. UV spektrá ukázali, že zlúčeniny la a lb obsahovali indolový skelet v molekule. Okrem toho ‚H-NMR spektrá ukázali, že zlúčeniny la a lb mali obidve indolový kruh s glykozidovou jednotkou v polohe 5 alebo 6. Tieto výsledky a hmotnostné spektrá naznačujú štruktúry zlúčenín la a lb
ako je znázornené na obr.
‚H-NMR spektrum zlúčeniny la bolo podobné spektru N,N-dimetylserotonín-5-0-Q-glukozidu, ktorý syntetizoval Krasavina ei at. 6 ) a izolované z listov Citrus unshiu v štúdii Nishida et al. o aktivite stimulácie vajíčok tryptamínových analógov motýľa lastovičníkovitého, ktorý sa živí Rutaceae.“ Naše údaje sú však mierne odlišné od ich spektrálnych údajov. Hoci N,N-dimetylserotonín-5-0-$-glukozid a jeho N-oxid boli izolované z tej istej rutóznej rastliny, neboli zaznamenané žiadne spektrálne údaje. 9 ) Preto sme syntetizovali ich acetylové deriváty, aby sme potvrdili tieto štruktúry (obr. 1).
Zlúčenina la sa acetylovala anhydridom kyseliny octovej v pyridíne, čím sa získal tetraacetát 2a s výťažkom 87 %. Hoci zlúčenina 2a už bola syntetizovaná a analyzovaná pomocou ‚H-NMR, naše1H -NMR údaje pre tetraacetát 2a sa líšili od ich údajov.
Acetyláciou zlúčeniny lb acetanhydridom/pyridínom sa získal pentaacetylovaný derivát zlúčeniny 2b okrem štyroch acetylových skupín na glykozidovej časti. Dva konforméry zlúčeniny 2b, ktoré vznikli v dôsledku prítomnosti amidovej skupiny, umožnili potvrdiť jej štruktúru pomocou hmotnostných a ‚H-NMR spektrálnych údajov pri 120 °C.
Kyslá hydrolýza zlúčeniny la alebo lb v 2 M HCI pri 70 °C počas 1 hodiny poskytla dimetylserotonín 3a (74 % výťažok z la) alebo monometylserotonín 3b (57 % výťažok z lb). Ich spektrálne údaje boli identické s údajmi syntetických 3a alebo 3b pripravených zo serotonínu metyláciou, hoci neboli totožné s údajmi uvádzanými v literatúre. 0 “Rozpor medzi našimi údajmi a údajmi z literatúry bol spôsobený silnou zásaditosťou týchto zlúčenín, pričom zlúčeniny uvedené v literatúre sa považujú za uhličitany
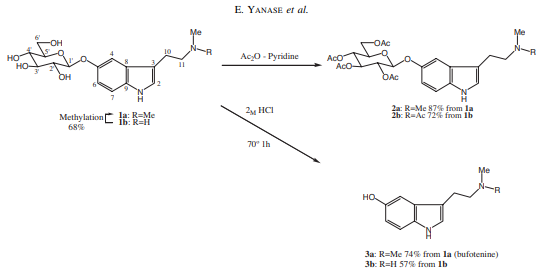
Obr. 1. Transformácia serotonínových analógov la a lb.
skôr amíny ako voľný amín. Skutočne, 3a a 3b poskytli ‚H-NMR údaje podobné tým, ktoré sú uvedené v literatúre po pridaní oxidu uhličitého alebo kyseliny octovej.
Štruktúry zlúčenín la a lb sa preto určili ako N,N-dimetyl-serotonín 5-0-$-glukozid a N-metylserotonín 5-0-
$-glukozid. Ďalej sa zlúčenina lb mohla previesť na la N-metyláciou, ktorá prebiehala s výťažkom 68,2 %. Príslušné obsahy la a lb v nezrelých semenách Z. piperitum boli odhadnuté na 0,299 c a 0,15 % (w/w) analýzou HPLC a ani jedna z týchto zlúčenín, ani ich aglykóny 3a a 3b neboli detegované v oplodiach.
Stručne povedané, zo semien Z. piperitum boli izolované dva analógy serotonínu a ich štruktúra bola určená ako N,N-dimetylserotonín 5-0-$-glukozid la a N-metylserotonín 5-0-Q-glukozid lb Dimetylderivát la bol prvýkrát izolovaný zo Z. piperitum spolu s novým monometylderivátom lb. Hladiny la a lb v semenách boli dostatočne vysoké, aby naznačovali, že môžu mať v tejto rastline nejaké neznáme dôležité funkcie. V súčasnosti študujeme vzťah medzi rastovým štádiom a endogénnymi hladinami týchto zlúčenín, aby sme ďalej objasnili ich biologický význam.
N,N-Dimetylserotonín 5-0-Q-glukozid la. Amorfné; ‚H-NMR H (600 MHz, Dz): 2,34 (6H, s, N-Me), 2,74 (2H, t, 7 = 7,8, H-10), 2,94 (2H, t, 7-7,8,
H-11), 3,49 (1H, t, 7 = 9,4, H-4′), 3,55-3,66 (3H, m,
H-2′, 3′, 5′), 3,75 (1H, dd, 7 = 6,0, 12,4, H-6′), 3,94
(1H, dd, 7 = 2,3, 12,4, H-6′), 5,07 (1 H, d, J- 7,3,
H-1′), 7,04 (1H, dd, 7-2,3, 8,7, H-6), 7,24 (1H, s,
H-2), 7,37 (1H, d, 7 = 2,3, H-4), 7,44 (1H, d, 7 = 8,7,
H-7); „C-NMR c (150 MHz, Dz): 24,8 (C-10), 46,4 (NC), 61,5 (C-11), 63,4 (C-6′), 72,3 (C-4′), 75,9 (C -2′),
78,4 (C-3′), 78,9 (C-5′), 104,7 (C-1′), 108,2 (C-4), 115,3
(C-3), 115,3 (C-7), 116,0 (C-6), 127,1 (C-2), 129,7
(C-8), 135,6 (C-9), 153,2 (C-5); UV max (MeOH) nm
(c): 278 (3,680), 220 (16,300); IR rp„ (KBr) cm*‘
2924, 2863, 1627, 1482, 1200, 1075, 1043; HR – ESI – MS
m/z: vypočítané pre C32H32N203S, 379,1; pre C8H27N26, 367,1869; nájdené, 367,1873; [ ]25D 32,07 (CI,0, Hz)
N-metylserotonín 5-0-$-glukozid lb. Amorfný;
’ H-NMR H (400 MHz, DzO): 2.49 (3H, s, N-Me), 3.04
(2H, br.d, 7 = 5,0, H-10), 3,08 (2H, br.d, 7 = 5,0,
H-11), 3,48 (1H, t, J – 9,4, H-4′), 3,56-3,61 (3H, m,
H-2′, 3′, 5′), 3,74 (1H, dd, 7 – 6,4, 12,4, H-6′), 3,94
(1H, dd, 7 = 1,8, 12,4, H – 6′), 5,09 (1H, d, 7 = 7,8,
H-1′), 7,06 (1 H, dd, 7 = 2,3, 9,2, H-6), 7,28 (1 H, s,
H-2), 7,37 (1H, d, J- 2,3, H-4), 7,45 (1H, d, J- 8,7, H-7); ‚C-NMR c (150 MHz, Dz): 25,5 (C-10), 36,3 (NC), 52,6 (C-11), 63,5 (C-6′), 72,4 (C-4‘), 75,9 (C -2′),
78,4 (C-3′), 78,9 (C-5′), 104,6 (C-1′), 108,1 (C-4), 113,4
(C-3), 115,4 (C-7), 116,1 (C-6), 127,9 (C-2), 129,6
(C-8), 135,7 (C-9), 153,3 (C-5); UV max (MeOH) nm
(c): 278 (4 700), 220 (21 400); IR rq „(KBr) cm * 1 ‚
2924, 1627, 1483, 1199, 1075, 1042; HR-ESI-MS m/z:
calcd. pre Ct H25N2 6› 353,1713; nájdené, 353,1719; [ ]° 5 D –30,63 (cl 0,0, Hz )
Poďakovanie
Ďakujeme pánovi Kazuhiko Naito z Hidasansyo Co., Ltd. za poskytnutie semien Zanthox ylum piperitum . Táto práca bola finančne podporená spoločnosťou Nagara Science Co., Ltd.
Referencie
- Yasuda I, Takeya K a Itokawa H, C/Iem Bull., 29, 1791-1793 (1981).
- Yasuda I, Takeya K a Itokawa H, Ph. tochemistrv, 21, 1295-1298 (1982).
- Yasuda I, Takeya K a Itokawa H, Sho jukugaku Zasshi, 36, 301-306 (1982).
- Jiang L a Kubota K, Agric. Fc›od Chem., 49, 1353-1357 (2001).
- Setzer WN, Noletto JA, Lawton RO a Harber WA, Divers., 9, 3-13 (2005).
Krasavina LS, Vigdorchik MM, Turchin KF a Suvorov NN,
Zhurnal Organicheskoi Khimii, 13, 1520-1527 (1977).
- Nishida R, Ohsugi T a Fukami H, Biol. Chem., 54, 1853-1855 (1990).
- Ohsugi T, Nishida R a Fukami H, Entomol.Zol ., 26, 29-40 (1991).
- Qu SI, Liu QW, Tan CH, Jiang SH a Zhu DY, Planta,
72, 264—266 (2006).
- Somei M, Yamada F, Kurauchi T, Nagahama Y, Hasegawa M, Yamada K, Teranishi S, Sato H a Kaneko C, Chem. Bull., 49, 87-96 (2001).
- Yamada F, Tamura M a Somei M, Heteroc ycles, 49, 451-457 (1998).




